Énoncé
Correction
Exercice 1
1.1. L’équation chimique modélisant la réaction de l’acide butanoïque avec l’eau
$$ C_{3} H_{7} C O_{2} H_{(a q)}+H_{2} O_{(l)} \quad \rightleftarrows \quad C_{3} H_{7} C O_{2(a q)}^{-}+H_{3} O_{(a q)}^{+} $$
1.2. Le tableau d’avancement
1.3. la valeur de l'avancement maximal $$\boldsymbol{x}_{\max }$$
L’eau est en excès, l’acide est le réactif limitant:
$$ \begin{array}{c} C_{A} V_{A}-x_{\max }=0 \quad \rightarrow \quad x_{\max }=C_{A} V_{A} \\ x_{\max }=2.10^{-3} \times 1=2.10^{-3} \mathrm{~mol} \end{array} $$
1.4. la valeur de l'avancement à l'état d’équilibre
D’après le tableau d’avancement:
$$ \begin{aligned} n_{e q}\left(H_{3} O^{+}\right)=x_{e q}=\left[H_{3} O^{+}\right] . V_{A} \rightarrow x_{e q}=10^{-p H} \cdot V_{A} \\ \rightarrow x_{e q}=10^{-3,76} \times 1 \end{aligned} $$
$$ \rightarrow \quad x_{e q}=1,74.10^{-4} \mathrm{~mol} $$
1.5. La valeur du taux d'avancement final $$ \boldsymbol{\tau}$$
$$ \begin{array}{c} \tau=\frac{x_{e q}}{x_{\max }} \\ \tau=\frac{1,74 \cdot 10^{-4}}{2 \cdot 10^{-3}}=0,0087<1 \rightarrow \tau=8,7 \% \end{array} $$
La réaction de l’acide butanoïque avec l’eau est imitée.
1.6. la valeur de la constante d'équilibre K
$$ K=\frac{\left[H_{3} O^{+}\right]_{e q} \cdot\left[C_{3} H_{7} C O_{2}^{-}\right]_{e q}}{\left[C_{3} H_{7} C O_{2} H\right]_{e q}} $$
D’après le tableau d’avancement:
$$ \begin{array}{c} {\left[\mathrm{H}_{3} \mathrm{O}^{+}\right]_{e q}=\left[\mathrm{C}_{3} \mathrm{H}_{7} \mathrm{CO}_{2}^{-}\right]_{e q}=\frac{\chi_{e q}}{V_{A}}=10^{-p H}} \\ {\left[\mathrm{C}_{3} \mathrm{H}_{7} \mathrm{CO}_{2}^{-}\right]_{e q}=\frac{C_{A} \cdot V_{A}-x_{e q}}{V_{A}}=C_{A}-\frac{x_{e q}}{V_{A}}=C_{A}-10^{-p H}} \\ K=\frac{\left[\mathrm{H}_{3} \mathrm{O}^{+}\right]_{e q}^{2}}{\left[C_{3} \mathrm{H}_{7} \mathrm{CO}_{2} \mathrm{H}\right]_{e q}}=\frac{\left(10^{-p H}\right)^{2}}{C_{A}-10^{-p H}}=\frac{10^{-2 p H}}{C_{A}-10^{-p H}} \\ K=\frac{10^{-2 \times 3,76}}{2 \cdot 10^{-3}-10^{-3,76}} \rightarrow K=1,65.10^{5} \end{array} $$
1.7.
1.8. la valeur du $$p K_{A}\left(C_{3} H_{7} C O_{2} H_{(a q)} / C_{3} H_{7} C O_{2(a q)}^{-}\right)$$
$$ \begin{array}{c} p K_{A}=-\log K_{A} \\ K=K_{A} \\ p K_{A}=-\log K=-\log \left(1,65.10^{-5}\right)=4,78 \end{array} $$
2.1. l’équation de la réaction du dosage
$$\mathrm{C}_{3} \mathrm{H}_{7} \mathrm{CO}_{2} \mathrm{H}_{(\mathrm{aq})}+\mathrm{HO}_{(\mathrm{aq})}^{-} \rightleftarrows \mathrm{C}_{3} \mathrm{H}_{7} \mathrm{CO}_{2(\mathrm{aq})}^{-}+\mathrm{H}_{2} \mathrm{O}_{(l)}$$
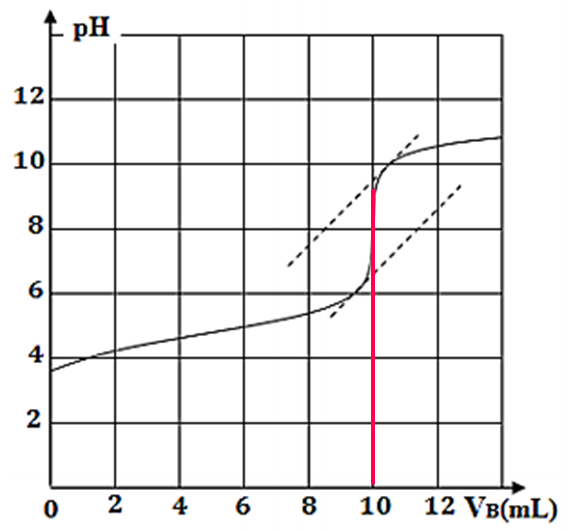
2.2. la valeur du volume $$V_{B, E}$$
$$V_{B, E}=10mL$$
2.3. la valeur de C
A l’équilibre, on a:
$$ \begin{array}{c} C . V=C_{B} \cdot V_{B, E} \\ C=\frac{C_{B} \cdot V_{B, E}}{V} \\ C=\frac{4.10^{-3} \times 10 \times 10^{-3}}{10.10^{-3}} \\ C=4.10^{-3} \mathrm{mol.} L^{-1} \end{array} $$
2.4. la masse de l’acide butanoïque
$$ \begin{aligned} n=C . V_{0}=& \frac{m}{M\left(C_{3} H_{7} C O_{2} H\right)} \quad \rightarrow \quad m=C . V_{0} \cdot M\left(C_{3} H_{7} C O_{2} H\right) \\ & \rightarrow m=4.10^{-3} \times 1 \times 88=0,352 g \end{aligned}$$
Le pourcentage d’acide butanoïque dans le beurre étudié:
$$ p=\frac{m}{m_{b}} \rightarrow p=\frac{0,352}{10}=0,0352 \quad \rightarrow \quad p=3,52 \% $$
Non, le beurre étudié n’est pas rance car $$ \mathrm{p}<4 \% $$.