الترتيب الدوري للعناصر الكيميائية
مع تزايد العناصر الكيميائية المكتشفة والمصنعة أصبح ترتيبها حسب معايير محددة ضرورة ملحة، ويعد ماندلييف أهم من أنجز ترتيبا دوريا سنة 1896م. وبعد تطور األبحاث واكتشاف أنواع جديدة استقر األمر على الترتيب الحالي والذي يضم 118عنصرا. إن أهم خصائص الترتيب الدوري للعناصر الكيميائية، هو تصنيف العناصر على شكل مجموعات كيميائية، حيث تتصف عناصر المجموعة الواحدة بخواص كيميائية متشابهة جدا.
I.الترتيب الدوري للعناصر الكيميائية
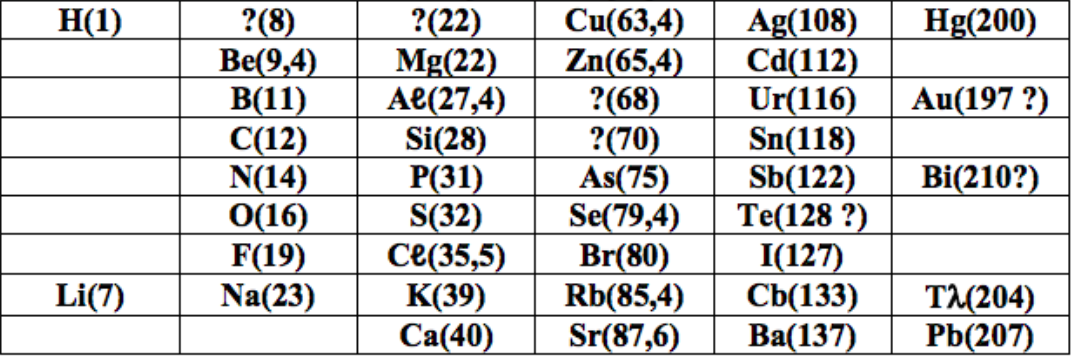
1.ترتيب ماندلييف

رتب ماندلييف العناصر الكيميائية المعروفة في زمانه حسب معيارين:
- تزايد الكتلة المولية للعناصر الكيميائية.
- الخواص الكيميائية للعناصر، حيث جمع في الصف األفقي الواحد عناصر لها خصائص كيميائية متشابهة.
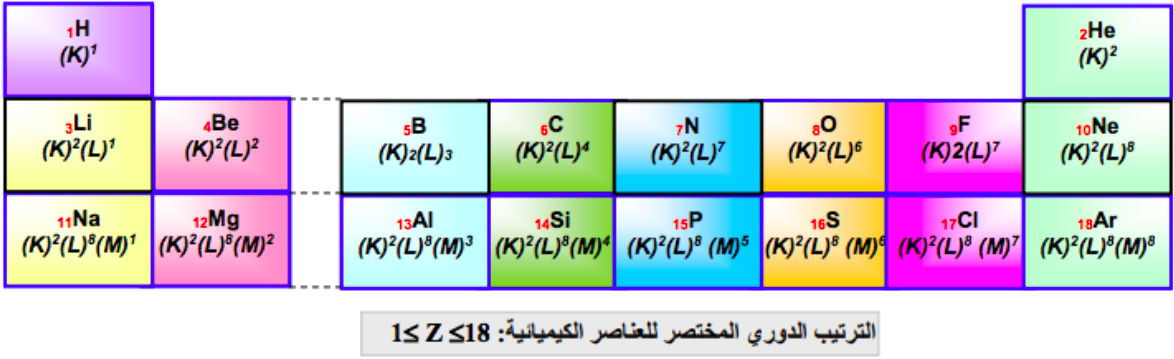
2.الترتيب الدوري الحالي:
يضم الجدول الحالي 118 عنصرا : آخر عنصر تم اكتشافه سنة 1999 وهو أونونوكتيوم Ununoctium ،رمزه المؤقت Uuo, مرتب حسب صفو أفقية، تسمى دوراتPériodes وعددها 7 ،وصفوف رأسية أعمدة Colonnes تسمى مجموعات وعددها 18 ،ويتميز هذا الترتيب بالخصائص التالية:
- ترتيب العناصر الكيميائية حسب تزايد العدد الذري Z
- توجد العناصر التي تحتوي ذراتها على نفس عدد االلكترونات في المستوى الخارجي على نفس العمود، وتسمى مجموعة Groupe.
- تحتوي ذرات العناصر الكيميائية، التي تنتمي لنفس الدورة على نفس عدد الطبقات االلكترونية.
استعمال الترتيب الدوري
لمواصلة هذا الملخص، قم بالتسجيل بالمجان في كيزاكو

النسخة المجانية لكيزاكو:
- ملخصات الدروس غير محدودة
- فيديو مجاني في كل درس
- تمرين مصحح مجاني
- اختبار تفاعلي